NEWS
NEWS
Gene crucial for growth of Ewing sarcoma uncovered
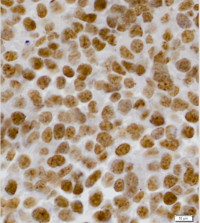
Pictured: Ewing sarcoma cells with RING1B activity highlighted in brown.
Researchers at the Centre for Genomic Regulation (CRG) and the Institut de Recerca Sant Joan de Déu (IRSJD) have discovered that RING1B is a critical gene for the development of Ewing sarcoma, a rare type of developmental cancer that presents in bones and soft tissues. This newly uncovered epigenetic vulnerability in Ewing sarcoma cancer cells opens the door for new therapeutic strategies.
Ewing sarcoma is caused by a chromosomal translocation, where the EWSR1 gene in chromosome 22 fuses with the FLI1 gene in chromosome 11. The resulting EWSR1-FLI1 fusion protein, which contains the transcriptional activation machinery of EWSR1 and the DNA-binding domain of FLI1, is the main driver of tumorigenesis.
A new study published today in Science Advances describes how the oncogenic EWSR1-FLI1 fusion protein is directed to the different parts of the genome by RING1B, allowing EWSR1-FLI1 to hijack the transcriptional program of the cells, turning them into cancerous cells.
Researchers found that RING1B and EWSR1-FLI1 localize at the same regions in the genome, where RING1B is responsible for EWSR1-FLI1 recruitment. EWSR1-FLI1 cannot activate its target genes and transform a cell from healthy to cancerous state without RING1B, as shown by impaired tumour growth when RING1B is reduced.
Epigenetic inhibitors have been previously proposed to treat Ewing sarcoma and other types of paediatric cancers such as neuroblastoma, rhabdomyosarcoma or synovial sarcoma. Further research could explore the pharmacological inhibition of RING1B as a clinical therapy to treat Ewing sarcoma.
“Our findings offer striking insights into the machinery of Ewing sarcoma, helping us get closer to uncovering the elusive cell-of-origin for this rare type of cancer,” says Luciano Di Croce, researcher at the Centre for Genomic Regulation and one of the authors of the study. “All we have to do is look for high levels of RING1B.”
“EWSR1-FLI1 remains a challenging druggable target, therefore understanding its dependencies may offer alternative strategies to switch off its aberrant transcriptional program,” says Sara Sánchez-Molina, first author of the study and postdoctoral researcher at the Institut de Recerca Sant Joan de Déu.
“Ewing tumors are paradigmatic examples of developmental cancers, where the first hit (genetic or epigenetic) occurs during embryonic development (gestation) and, in the majority of Ewing sarcomas, develops postnatally during specific stages of growth like puberty. The study supports the model by which embryonic stem cells characterized by high levels of RING1B are capable to sustain the aberrant transcriptional program caused by the oncogenic fusion protein. Ewing sarcoma will develop if the individual is born with precursor cells bearing the fusion oncoprotein”, says Jaume Mora, Scientific Director of the Pediatric Cancer Center Barcelona - Institut de Recerca Sant Joan de Déu, and director of the study.
ABOUT THE CRG
The Centre for Genomic Regulation (CRG) is an international biomedical research institute of excellence, based in Barcelona. The mission of the CRG is to discover and advance knowledge for the benefit of society, public health and economic prosperity. Its interdisciplinary scientific team (over 400 scientists) is focused on understanding the complexity of life from the genome to the cell to a whole organism and its interaction with the environment. The CRG is part of The Barcelona Institute of Science and Technology (BIST) and it is a CERCA centre from the Government of Catalonia.
EN ESPAÑOL
Descubierto un gen crucial para el desarollo del sarcoma de Ewing
Investigadores del Institut de Recerca Sant Joan de Déu (IRSJD), en colaboración con el Centro de Regulación Genómica (CRG), han descubierto que el gen RING1B es crítico para el desarrollo del sarcoma de Ewing, un tipo de cáncer poco frecuente que se presenta en los huesos y tejidos blandos.
Esta nueva vulnerabilidad epigenética en las células cancerosas del sarcoma de Ewing abre la puerta al desarrollo de nuevas estrategias terapéuticas.
El sarcoma de Ewing es causado por una translocación cromosómica, donde el gen EWSR1 en el cromosoma 22 se fusiona con el gen FLI1 en el cromosoma 11. La proteína de fusión resultante, llamada EWSR1-FLI1, es el principal impulsor de la tumorigénesis gracias a la maquinaria de activación transcripcional de EWSR1 y el dominio de unión al ADN de FLI1.
Un nuevo estudio publicado hoy en Science Advances describe cómo la proteína de fusión oncogénica EWSR1-FLI1 está dirigida a las diferentes partes del genoma por RING1B, permitiendo que EWSR1-FLI1 secuestre el programa transcripcional de las células, convirtiéndolas en células cancerosas.
Los investigadores encontraron que RING1B y EWSR1-FLI1 se localizan en las mismas regiones del genoma, donde RING1B es responsable del reclutamiento de EWSR1-FLI1. EWSR1-FLI1 no puede activar sus genes diana y transformar una célula sana a una cancerosa sin RING1B. Los investigadores mostraron que los tumores crecían peor cuando se reducía la expresión de RING1B.
Se han propuesto previamente inhibidores epigenéticos para tratar el sarcoma de Ewing y otros tipos de cánceres pediátricos como el neuroblastoma, el rabdomiosarcoma o el sarcoma sinovial. Futuras investigaciones pueden explorar la inhibición farmacológica de RING1B como terapia clínica para tratar el sarcoma de Ewing.
"Nuestros hallazgos ofrecen información sorprendente sobre la maquinaria del sarcoma de Ewing, acercándonos a descubrir por fin la célula de origen de este tipo de cáncer raro", dice Luciano Di Croce, investigador del Centro de Regulación Genómica y uno de los autores del estudio. "Todo lo que tenemos que hacer es buscar niveles altos de RING1B".
“EWSR1-FLI1 sigue siendo una diana terapéutica desafiante, por lo que comprender sus dependencias puede ofrecer estrategias alternativas para desconectar su programa transcripcional aberrante”, dice Sara Sánchez-Molina, primera autora del estudio e investigadora postdoctoral en el Institut de Recerca Sant Joan de Déu.
“Los tumores de Ewing son ejemplos paradigmáticos de cánceres del desarrollo, donde el primer golpe (genético o epigenético) ocurre durante el desarrollo embrionario (gestación) y, en la mayoría de los sarcomas de Ewing, se desarrolla postnatalmente durante etapas específicas de crecimiento como la pubertad. El estudio apoya el modelo por el cual las células madre embrionarias caracterizadas por altos niveles de RING1B son capaces de mantener el programa transcripcional aberrante causado por la proteína de fusión oncogénica. El sarcoma de Ewing se desarrollará si el individuo nace con células precursoras portadoras de la oncoproteína de fusión”, afirma Jaume Mora, director científico del Centro Oncológico Pediátrico Barcelona - Institut de Recerca Sant Joan de Déu, y director del estudio.
SOBRE EL CRG
El Centro de Regulación Genómica (CRG) es un centro internacional de investigación biomédica de excelencia, ubicado en Barcelona. Su misión es descubrir y promover el conocimiento en beneficio de la sociedad, la salud pública y la prosperidad económica. Su equipo científico interdisciplinar (de más de 400 miembros) está centrado en comprender la complejidad de la vida, desde el genoma hasta la célula y un organismo completo, y su interacción con el entorno. El CRG forma parte de The Barcelona Institute of Science and Technology (BIST) y es un centro CERCA de la Generalitat de Catalunya.
EN CATALÀ
Descobert un gen crucial per al desenvolupament del sarcoma d'Ewing
Investigadors de l'Institut de Recerca Sant Joan de Déu (IRSJD), en col·laboració amb el Centre de Regulació Genòmica (CRG), han descobert que el gen RING1B és crític per al desenvolupament del sarcoma d'Ewing, un tipus de càncer poc freqüent que es presenta en els ossos i teixits tous.
Aquesta nova vulnerabilitat epigenètica en les cèl·lules canceroses del sarcoma d'Ewing obre la porta al desenvolupament de noves estratègies terapèutiques.
El sarcoma d'Ewing és causat per una translocació cromosòmica, on el gen EWSR1 en el cromosoma 22 es fusiona amb el gen FLI1 en el cromosoma 11. La proteïna de fusió resultant, anomenada EWSR1-FLI1, és el principal impulsor de la tumorigènesi gràcies a la maquinària d'activació transcripcional de EWSR1 i el domini d'unió a l'ADN de FLI1.
Un nou estudi publicat avui a Science Advances descriu com la proteïna de fusió oncogènica EWSR1-FLI1 està dirigida a les diferents parts del genoma per RING1B, permetent que EWSR1-FLI1 segresti el programa transcripcional de les cèl·lules, convertint-les en cèl·lules canceroses.
Els investigadors van trobar que RING1B i EWSR1-FLI1 es localitzen en les mateixes regions del genoma, on RING1B és responsable del reclutament d’EWSR1-FLI1. EWSR1-FLI1 no pot activar els seus gens diana i transformar una cèl·lula sana en una cancerosa sense RING1B. Els investigadors van mostrar que els tumors creixien pitjor quan es reduïa l'expressió de RING1B.
S'han proposat prèviament inhibidors epigenètics per tractar el sarcoma d'Ewing i altres tipus de càncers pediàtrics com el neuroblastoma, el rabdomiosarcoma o el sarcoma sinovial. Futures investigacions poden explorar la inhibició farmacològica de RING1B com a teràpia clínica per tractar el sarcoma d'Ewing.
"La nostra recerca ofereix informació sorprenent sobre la maquinària del sarcoma d'Ewing, apropant-nos a descobrir per fi la cèl·lula d'origen d'aquest tipus de càncer rar", diu Luciano Di Croce, investigador de el Centre de Regulació Genòmica i un dels autors de l'estudi. "Tot el que hem de fer és buscar nivells alts de RING1B".
"EWSR1-FLI1 segueix sent una diana terapèutica desafiant, per la qual cosa comprendre les seves dependències pot oferir estratègies alternatives per a desconnectar el seu programa transcripcional aberrant", diu Sara Sánchez-Molina, primera autora de l'estudi i investigadora postdoctoral a l'Institut de Recerca Sant Joan de Déu.
"Els tumors d'Ewing són exemples paradigmàtics de càncers del desenvolupament, on el primer cop (genètic o epigenètic) succeeix durant el desenvolupament embrionari (gestació) i, en la majoria dels sarcomes d'Ewing, es desenvolupa postnatalment durant etapes específiques de creixement com la pubertat. L'estudi dóna suport al model pel qual les cèl·lules mare embrionàries caracteritzades per alts nivells de RING1B són capaces de mantenir el programa transcripcional aberrant causat per la proteïna de fusió oncogènica. El sarcoma d'Ewing es desenvoluparà si l'individu neix amb cèl·lules precursores portadores de la oncoproteïna de fusió", afirma Jaume Mora, director científic de el Centre Oncològic Pediàtric Barcelona - Institut de Recerca Sant Joan de Déu, i director de l'estudi.
SOBRE EL CRG
El Centre de Regulació Genòmica (CRG) és un institut internacional de recerca biomèdica d’excel·lència, ubicat a Barcelona. La seva missió és descobrir i promoure el coneixement en benefici de la societat, la salut pública i la prosperitat econòmica. El seu equip científic interdisciplinari (de més de 400 membres) se centra en comprendre la complexitat de la vida, des del genoma fins a la cèl·lula i un organisme complet, i la seva interacció amb l’entorn. El CRG forma part de The Barcelona Institute of Science and Technology (BIST) i és un centre CERCA de la Generalitat de Catalunya.