NOTICIAS
NOTICIAS
Tiny gene fragments revealed as crucial new players in retinal development and vision
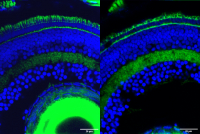
Retinal cells in zebrafish with the outer segment, the part of photoreceptor cells responsible for transforming light into nervous signals that enable vision, stained in green at the top of the image. The outer segment is significantly degraded in retinal cells with the Srrm3 gene knocked out (right) compared to normal retinal cells (left). Credit: Ludovica Ciampi/CRG/Proceedings of the National Academy of Sciences
Researchers at the Centre for Genomic Regulation (CRG) in Barcelona reveal that Srrm3 is a master regulator gene crucial for the development of photoreceptors, cells in the back of the retina which capture and process light, sending signals to the brain that enable vision. Knocking the gene out in zebrafish resulted in severe visual impairment.
The research found that, in vertebrates, Srrm3 works by regulating alternative splicing, a process that allows cells to make more than one type of protein from a single gene and is particularly prominent in neuronal cells. The misregulation of alternative splicing can have a devastating impact on human health, for example in cancer or neurological disorders.
Srrm3 was found to specifically regulate the splicing of microexons, tiny fragments of DNA that are just 3-27 letters long. Despite their small size, the regulation of microexons has been shown to play a critical role in protein and cellular function.
The researchers identified dozens of different microexons that are mainly present in photoreceptors but not in other neurons. A large proportion of these microexons affect the function of around 70 genes important for the development of a photoreceptor’s outer segment, the part of the cell that absorbs light. The findings are published in the Proceedings of the National Academy of Sciences.
The study reveals a new layer of cellular specialisation required for the unique cellular shape and function of retinal cells, one of the most complex and specialised cells in the human body. Because of this complexity, retinal cells depend on many unique genes for their development, any which of can have a disease-causing mutation and result in vision loss.
One of the most common causes of inherited vision loss is retinitis pigmentosa, a genetic disorder for which the molecular mechanisms involved are poorly understood. Between 40 to 50 percent of cases of retinitis pigmentosa have no explanation, meaning they carry mutations in genes yet to be identified. The authors of the study plan on carrying out future studies to assess whether Srrm3 or the microexons involved could explain some of these cases.
“The Srrm3 gene has neither been associated with the development of photoreceptor cells nor with the pathogenesis of retinal diseases before. We are already exploring the gene’s role in patients without a genetic diagnosis. If we find cases with mutations in this specific gene, or on any retinal microexons, it could lead to potential new therapeutic strategies to manage the condition,” says Ludovica Ciampi, PhD student at the CRG and first author of the study.
According to ICREA Research Professor Manuel Irimia, understanding microexon regulation in specific cell types is key for identifying new therapeutic targets. “Photoreceptors have unique properties thanks to the regulation of alternative splicing and microexons. This helps make the cell more specialised but also perhaps more susceptible to genetic diseases. Modulating splicing activity is now possible, so the more intricate biology we uncover, the more likely we are to find therapeutic targets to treat retinal diseases,” concludes Dr. Irimia.
The study is a result of a collaboration between ICREA Research Professors Luis Serrano and Manuel Irimia at the CRG, as well as the Telethon Institute of Genetics and Medicine of Naples, Italy and the University of Zurich in Switzerland. The work is funded by the European Research Council, Spanish Ministry of Science and Innovation and the Generalitat de Catalunya.
EN CASTELLANO
Identifican pequeños fragmentos de genes cruciales para el desarrollo de la retina y la visión
Un equipo científico del Centro de Regulación Genómica (CRG), en Barcelona revela que Srrm3 es un gen regulador maestro crucial para el desarrollo de los fotorreceptores –células en la parte posterior de la retina que capturan y procesan la luz, enviando señales al cerebro que activan la visión. La eliminación de este gen en el pez cebra resultó en una discapacidad visual grave.
La investigación descubrió que, en los vertebrados, Srrm3 regula el empalme alternativo, un proceso que permite a las células producir más de un tipo de proteína a partir de un solo gen. La actividad del empalme alternativo es particularmente prominente en las células neuronales, y su mala regulación puede tener un impacto devastador en la salud humana, por ejemplo, en el cáncer o los trastornos neurológicos.
Se descubrió que Srrm3 regula específicamente el empalme de microexones, pequeños fragmentos de ADN que tienen solo entre 3 y 27 letras de largo. A pesar de su pequeño tamaño, se ha demostrado que la regulación de los microexones desempeña un papel fundamental en la función proteica y celular.
El equipo científico pudo identificar docenas de microexones diferentes en los fotorreceptores pero no así en otras neuronas. La gran mayoría de estos microexones afectan a la función de unos 70 genes importantes para el desarrollo del segmento externo de un fotorreceptor, la parte de la célula que absorbe la luz. Los hallazgos del estudio se publican en la revista Proceedings of the National Academy of Sciences.
Las células retinianas son unas de las células más complejas y especializadas del cuerpo humano. El estudio revela los mecanismos que hacen que esta especialización sea posible. Debido a esta complejidad, las células de la retina dependen de muchos genes únicos para su desarrollo, cualquiera de los cuales puede tener una mutación que cause una enfermedad y resulte en la pérdida de la visión.
Una de las causas más comunes de pérdida hereditaria de la visión es la retinosis pigmentaria, un trastorno genético en el cual se conocen poco los mecanismos moleculares implicados. Entre el 40 y el 50 por ciento de los casos de retinosis pigmentaria no tienen explicación, lo que significa que portan mutaciones en genes aún por identificar. Los autores del estudio planean realizar estudios de seguimiento para evaluar si Srrm3 o los microexones implicados podrían explicar algunos de estos casos.
“Hasta ahora, el gen Srrm3 no se había asociado con el desarrollo de células fotorreceptoras ni con la patogenia de enfermedades de la retina. Ya estamos explorando el rol del gen en pacientes sin diagnóstico genético. Si encontramos casos con mutaciones en este gen específico, o en cualquier microexón de la retina, esto nos podría llevar a posibles nuevas estrategias terapéuticas para controlar la afección”, afirma Ludovica Ciampi, estudiante de doctorado en el CRG y primera autora del estudio.
Según el profesor de investigación ICREA Manuel Irimia, la comprensión de cómo se regulan los microexones en diferentes tipos de células será clave para identificar nuevas dianas terapéuticas. “Los fotorreceptores tienen propiedades únicas gracias a la regulación del empalme alternativo y los microexones. Esto ayuda a que la célula sea más especializada pero también quizás más susceptible a enfermedades genéticas. Ahora es posible modular la actividad de empalme, por lo que cuanto más sepamos de esta compleja biología, más probable será que encontremos dianas terapéuticas para tratar enfermedades de la retina”, concluye el Dr. Irimia.
El estudio es el resultado de una colaboración entre los profesores de investigación ICREA Luis Serrano y Manuel Irimia en el CRG, así como el Instituto Teletón de Genética y Medicina de Nápoles, Italia; y la Universidad de Zúrich en Suiza. El trabajo está financiado por el Consejo Europeo de Investigación, el Ministerio de Ciencia e Innovación de España y la Generalitat de Catalunya.
EN CATALÀ
Identifiquen petits fragments de gens crucials per al desenvolupament de la retina i la visió
Un equip científic del Centre de Regulació Genòmica (CRG), a Barcelona, revela que Srrm3 és un gen regulador mestre crucial per al desenvolupament dels fotoreceptors –cèl·lules a la part posterior de la retina que capturen i processen la llum, enviant senyals al cervell que activen la visió. L’eliminació d’aquest gen en el peix zebra resultà en una discapacitat visual greu.
La recerca descobrí que, en els vertebrats, Srrm3 regula l’empalmament alternatiu, un procés que permet a les cèl·lules produir més d’un tipus de proteïna a partir d’un sol gen. L’activitat de l’empalmament alternatiu és particularment prominent a les cèl·lules neuronals, i una mala regulació pot tenir un impacte devastador en la salut humana, com ara, en el càncer o els trastorns neurològics.
Es descobrí que Srrm3 regula específicament l’empalmament de microexons, petits fragments d’ADN que tenen només entre 3 i 27 lletres de llarg. Tot i les seves reduïdes dimensions, s’ha demostrat que la regulació dels microexons exerceix un paper fonamental en la funció proteica i cel·lular.
L’equip científic pogué identificar dotzenes de microexons diferents en els fotoreceptors, però no així en d’altres neurones. La gran majoria d’aquests microexons afecten la funció d’uns 70 gens importants per al desenvolupament del segment extern d’un fotoreceptor, la part de la cèl·lula que absorbeix la llum. Les troballes de l’estudi es publiquen a la revista Proceedings of the National Academy of Sciences.
Les cèl·lules retinals són unes de les cèl·lules més complexes i especialitzades del cos humà. L’estudi revela els mecanismes que fan que aquesta especialització sigui possible. A causa d’aquesta complexitat, les cèl·lules de la retina depenen de molts gens únics per al seu desenvolupament, i qualsevol d’ells pot tenir una mutació que causi una malaltia i resulti en la pèrdua de la visió.
Una de les causes més comunes de pèrdua hereditària de la visió és la retinosi pigmentària, un trastorn genètic en què es coneixen poc els mecanismes moleculars implicats. Entre el 40 i el 50 per cent dels casos de retinosi pigmentària no tenen explicació, fet que significa que porten mutacions en gens que encara no s’han identificat. Els autors de l’estudi planegen realitzar estudis de seguiment per avaluar si Srrm3 o els microexons implicats podrien explicar alguns d’aquests casos.
“Fins ara, el gen Srrm3 no s’havia associat amb el desenvolupament de cèl·lules fotoreceptores ni amb la patogènia de malalties de la retina. Ja estem explorant el rol del gen en pacients sense diagnòstic genètic. Si trobem casos amb mutacions en aquest gen específic, o en qualsevol microexó de la retina, això ens podria dur a possibles noves estratègies terapèutiques per a controlar l’afecció”, afirma Ludovica Ciampi, estudiant de doctorat al CRG i primera autora de l’estudi.
Segons el professor d’investigació ICREA Manuel Irimia, la comprensió de cóm es regulen els microexons en diferents tipus de cèl·lules serà clau per a identificar noves dianes terapèutiques. “Els fotoreceptors tenen propietats úniques gràcies a la regulació de l’empalmament alternatiu i els microexons. Això ajuda a què la cèl·lula sigui més especialitzada, però també pot ser més susceptible a malalties genètiques. Ara és possible modular l’activitat de l’empalmament i, per tant, quant més coneixement tinguem d’aquesta complexa biologia, més probable serà que trobem dianes terapèutiques per a tractar malalties de la retina”, conclou el Dr. Irimia.
L’estudi és el resultat d’una col·laboració entre els professors d’investigació ICREA Luis Serrano i Manuel Irimia al CRG, i també de l’Institut Teleton de Genètica i Medicina de Nàpols, Itàlia; i la Universitat de Zurich, a Suïssa. El treball està finançat pel Consell Europeu de Recerca, el Ministeri de Ciència i Innovació espanyol i la Generalitat de Catalunya.